
13YR企业会员
发布人:深圳振强生物技术有限公司
发布日期:2026/4/17 11:42:09


就在2026年3月,Appco Pharma LLC自愿召回175,061瓶盐酸哌唑嗪胶囊(规格为1mg、2mg、5mg)。而仅隔5个月前,即2025年10月,Teva制药也曾召回超过58万瓶该药品。
那么问题来了,两次来自不同公司的产品独立召回,究竟是什么让两家企业不约而同触发安全预警?其实这并非偶然,“真正的元凶”就是—N-亚硝基-哌唑嗪EP杂质C(N-Nitroso-Prazosin EP Impurity C)超标。

01 N-亚硝基-哌唑嗪EP杂质C:化学身份与结构关系
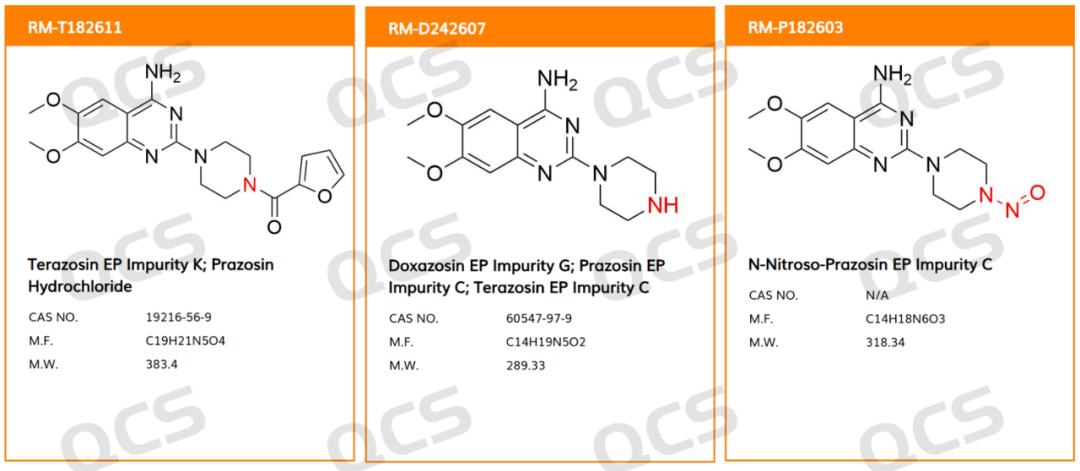
“导致本次召回的元凶—N-亚硝基-哌唑嗪EP杂质C,该杂质是哌唑嗪 EP 杂质 C(Prazosin EP Impurity C)的亚硝胺产物。”
哌唑嗪EP杂质C : 非亚硝基形式;QCS货号:RM-D242607
6,7-Dimethoxy-2-(piperazin-1-yl)quinazolin-4-amine,同时是多沙唑嗪(EP杂质G)和特拉唑嗪(EP杂质C)的杂质。由于哌唑嗪EP杂质C含有哌嗪环(piperazine)结构,本质为一个仲胺(secondary amine)。相比原料药更容易发生亚硝胺化反应,是潜在的亚硝胺前体。
前体哌唑嗪杂质C的来源很广泛,可能包括中间体残留杂质,API降解过程或在制剂环境中的二次生成。哌唑嗪EP杂质C的存在往往很难避免。
N-亚硝基-哌唑嗪EP杂质C:亚硝基形式;QCS货号:RM-P182603
是上述非亚硝基杂质的N-亚硝基衍生物(哌嗪环氮原子发生N-亚硝基化)。由于唑嗪EP杂质C同时也存在多沙唑嗪和特拉唑嗪药物中,因此这两种药物中也有可能存在N-亚硝基-哌唑嗪EP杂质C,在这些药物的研究中该杂质也需要被加以关注。
02 特定亚硝胺形成机理与风险特征
3.1 亚硝化反应路径
在API合成或制剂储存过程中,哌唑嗪或其非亚硝基杂质(含仲胺/叔胺片段)与亚硝化试剂(如亚硝酸盐,可来源于辅料、包材或环境)反应:
R2NH+NO2-(酸性条件)→R2N–NO
该反应在酸性pH(尤其pH 3~4)下最易发生。对于哌嗪环,亚硝化可发生在任一氮原子上,生成N-亚硝基哌嗪衍生物。
3.2 NDSRI的特殊风险
来源双重性:既可能是API合成中引入的工艺杂质,也可能是制剂中次生形成的降解杂质。
货架期增长:部分NDSRI在成品稳定性考察中呈上升趋势,提示需关注制剂环境(水分、pH、辅料、温度)。
结构活性不确定性:多数NDSRI无完整毒理学数据,监管机构采用CPCA(Carcinogenic Potency Categorization Approach),基于结构相似性预测其致癌效力并计算临时限度(如哌唑嗪召回中采用的5ppm即为基于CPCA的限度)。
03 监管要求

哌唑嗪的连续两次召回,清晰揭示了NDSRI控制的复杂性与紧迫性—杂质可能源于API,也可能在制剂中“生长”;没有标准品,就无法建立方法,更谈不上可靠的风险评估。
根据加州药房委员会(California State Board of Pharmacy)的资料,该杂质的可接受限值为5 ppm,2025年和2026年两次召回均是由于N-亚硝基-哌唑嗪EP杂质C的含量超过安全限值,被FDA定性为Class II风险召回。频繁重复出现的类似召回现象,意味着同一API / 同一结构类型 / 同一类杂质问题,正在“重复发生”。更需要注意的是:这两次涉及的杂质N-亚硝基-哌唑嗪EP杂质C,并非原始设计杂质,而是“衍生杂质”。
越来越多的示例说明,监管机构对亚硝胺警示结构的关注点已经从简单的API本身亚硝胺,延伸至杂质组分的亚硝胺风险评估。FDA及USP亚硝胺社区重点讨论:杂质可能不仅在API中残留,更可能在制剂成品中形成或增长,因此对于对含哌嗪/哌啶结构的药物,NDSRI的全过程控制已成为监管新常态。在监管机构将目光从NDMA转向NDSRIs的背景下,高纯度、结构确证完备的亚硝胺杂质标准品,已成为含胺类药物全生命周期质量控制的基础设施之一。
如需获取N-亚硝基-哌唑嗪EP杂质C(RM-P182603)或其他NDSRI标准品的技术资料与报价,欢迎联系QCS药物研发中心。
QCS已取得ANAB ISO 17034认可,标准品生产与定值过程符合国际参考物生产者能力认可要求,为NMPA、EMA、FDA等监管申报提供具备国际互认效力的数据支撑。



相关新闻资讯