
7YR企业会员
发布人:爱必信(上海)生物科技有限公司
发布日期:2026/4/17 13:40:07
体内巨噬细胞清除实验的核心是特异性去除巨噬细胞群体,同时最大程度减少对其他免疫细胞和组织的影响,氯膦酸二钠脂质体(Clodronate Liposomes)清除法是目前特异性最高、应用最广泛的体内巨噬细胞清除方法,几乎不影响中性粒细胞、淋巴细胞等其他细胞。
一、核心原理
氯膦酸二钠本身难以穿透细胞膜,被包裹进脂质体后,可通过巨噬细胞的吞噬作用被摄入胞内;脂质体在巨噬细胞溶酶体中被降解,释放出氯膦酸二钠,抑制细胞内 ATP 合成,最终诱导巨噬细胞凋亡。未被巨噬细胞吞噬的脂质体则会被肝脾代谢,对机体无明显毒性。
二、操作流程
步骤
具体操作
关键参数
试剂准备
选择商品化氯膦酸二钠脂质体(推荐规格:5 mg/mL 氯膦酸二钠),或实验室自制(需验证包封率>80%);同时准备空白脂质体作为对照
商品化试剂稳定性更高,避免自制脂质体包封率低导致的清除效率不足
动物与给药途径
适配小鼠、大鼠等常用实验动物;根据靶向部位选择给药方式:①全身巨噬细胞清除:尾静脉注射;②腹腔巨噬细胞清除:腹腔注射;③肺部巨噬细胞清除:气管内滴注;④肠道巨噬细胞清除:尾静脉/腹腔注射(结合肠道组织取材验证)
静脉注射起效最快(24 h 可见显著清除),局部注射靶向性更强
给药剂量与时间
常规剂量:- 小鼠:100–200 μL/只(含 0.2–0.4 mg 氯膦酸二钠),单次注射可维持 3–7 天清除效果;- 大鼠:按体重比例放大(5–10 mL/kg)实验周期>7 天:可间隔 5–7 天重复注射一次
剂量过高可能导致肝脾轻微损伤,需预实验优化
清除效率验证
注射后 24–48 h 取材检测,方法包括:①流式细胞术:检测组织单细胞悬液中巨噬细胞标志物(小鼠:CD11b⁺F4/80⁺;大鼠:CD11b⁺ED2⁺)的阳性率变化②免疫组化/免疫荧光:组织切片染色,观察巨噬细胞数量变化③ 功能验证:检测巨噬细胞吞噬功能(如荧光微球吞噬实验)
清除效率需达到 70% 以上,方可认为模型构建成功
三、优势与注意事项
1、优势
特异性强、毒性低、高活性、高稳定性、使用便捷、支持多种给药途径(静脉/腹腔/皮下/鼻内等)、清除效果可逆(停药后 2–3 周巨噬细胞可恢复正常水平)。
2、注意事项
必须设置空白脂质体对照组,排除脂质体本身对实验的影响;
避免反复高频注射,否则可能引发轻微炎症反应;
对破骨细胞等巨噬细胞谱系细胞也有清除作用,若实验关注骨代谢需谨慎使用。
3、使用方法:
具体注射方案可根据自身实验参考文献确定和优化,此处提供一种可参考的腹腔注射操作。
① 注射前,将Clodronate Liposomes(abs90559)和PBS Liposomes(abs90560)从冰箱取出,并回温到室温,但注意温度不能超过30°C。
② 将Clodronate Liposomes和PBS Liposomes都上下颠倒8-10次混匀。随后将26 Gauge针头装到1 mL注射器上吸取脂质体。吸取Clodronate Liposomes和PBS Liposomes的注射器不能混用。
注意:Clodronate Liposomes和PBS Liposomes 用前一定要充分混匀,不然可能影响实验效果。颠倒混匀时需要轻轻混匀,尽量避免起泡沫。
③ 用左手抓住小鼠并固定住小鼠头部和四肢。随后将小鼠微微倾斜,让头朝向地面,使得集中在腹部的器官向头部移动,远离注射位点。
④ 注射前将注射器颠倒6次,再次混匀脂质体。
注意:长时间静置可能会使脂质体在注射器中沉淀,所以用前需要再次混匀。
⑤ 针头30度斜插入小鼠腹部右下方,根据实验分组分别注射Clodronate Liposomes(实验组)和PBS Liposomes(对照组),每只小鼠注射200 μL脂质体。
四、文献应用分享
靶向肿瘤相关巨噬细胞(TAM)的功能研究解决方案
推荐模型:小鼠MC38(C57BL/6背景)或CT26(BALB/c背景)结直肠癌细胞系皮下或腹腔种植模型。
基因工程模型:采用髓系细胞特异性敲除小鼠(如Ccl7 MKO小鼠),用于研究特定基因在巨噬细胞中的功能。
2. 核心干预手段:巨噬细胞清除与靶向调控
氯膦酸盐脂质体清除法
方案:在肿瘤接种前1天,腹腔注射氯膦酸盐脂质体(200μL),之后每3天注射一次。
目的:直接验证巨噬细胞整体在肿瘤生长和免疫治疗应答中的必要性。
特异性靶点干预:
CCL7中和抗体:腹腔注射,100μg/次,每3天一次,用于阻断CCL7功能。
小分子抑制剂(如Bindarit,abs810272):口服灌胃,5 mg/kg,每3天一次,用于抑制CCL7表达。
联合治疗:与抗PD-L1抗体(200μg,腹腔注射)联用,评估协同抗肿瘤效果。
3. 多维度评价与验证体系
验证维度
核心检测指标
推荐技术与产品
解决方案对应目的
模型有效性
肿瘤生长曲线、小鼠生存期
活体成像系统、游标卡尺
评估干预手段的抗肿瘤效果
免疫细胞浸润分析
TAM (F4/80+CD11b+)、CD8+ T细胞、M1/M2亚型 (iNOS/Arg1)
流式细胞术(FCM)、免疫荧光/组化
量化免疫微环境重塑效果
功能性T细胞评估
IFN-γ+ CD8+ T细胞、Granzyme B+ CD8+ T细胞
流式细胞术(胞内染色)
评估细胞毒性免疫功能恢复情况
代谢与信号通路
脂质含量(Bodipy)、线粒体功能(OCR)、PEX3/PI3K/AKT/STAT1蛋白表达
Seahorse代谢分析、Western Blot、免疫荧光
阐明CCL7调控TAM免疫抑制功能的分子机制
趋化因子网络
CCL7、CXCL10等因子在血清或细胞上清中的浓度
ELISA试剂盒
验证CCL7对T细胞招募的抑制作用
巨噬细胞清除验证:使用氯膦酸盐脂质体清除巨噬细胞后,完全消除了外源性CCL7的促瘤作用,直接证明了CCL7的功能依赖于巨噬细胞的存在。
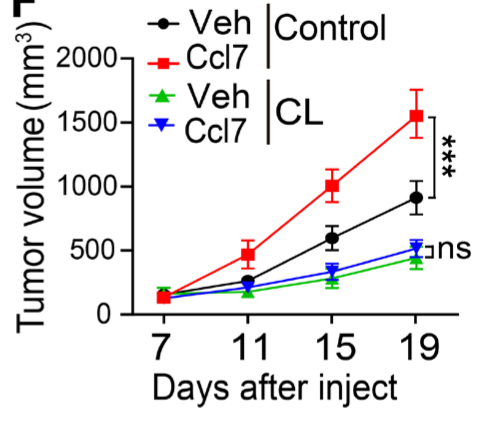 图1 小鼠皮下接种 MC38 肿瘤细胞后,腹腔注射氯膦酸脂质体或对照脂质体,并检测肿瘤体积。
图1 小鼠皮下接种 MC38 肿瘤细胞后,腹腔注射氯膦酸脂质体或对照脂质体,并检测肿瘤体积。
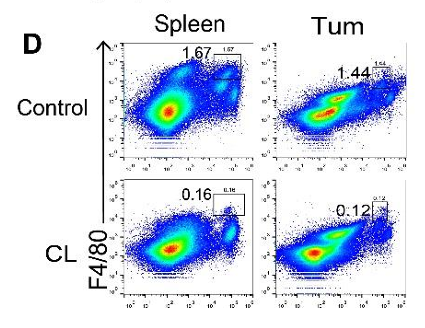 图2 流式细胞术检测肿瘤组织中F4/80+巨噬细胞的比例显著下降。
图2 流式细胞术检测肿瘤组织中F4/80+巨噬细胞的比例显著下降。
靶向CCL7的效果:使用中和抗体或抑制剂(Bindarit)靶向CCL7,可抑制肿瘤生长,延长生存期;减少TAM浸润,并促进其向M1样表型(iNOS+)转变;显著增加肿瘤内具有杀伤功能的CD8+ T细胞(IFN-γ+)浸润。
联合治疗优势:抗CCL7与抗PD-L1联合治疗展现出显著的协同效应,抗肿瘤效果和生存获益均优于单一疗法,为临床转化提供了强有力依据。
五、关键成功因素总结
脂质体质量:选择商业化的稳定制剂(如Absin abs90559)
注射技术:确保准确进入目标腔室,避免渗漏
混合均匀:注射前充分混匀脂质体,防止沉淀
验证步骤:必须通过组织学或流式确认清除效率
对照严谨:至少设置PBS和空脂质体双重对照
时间把握:根据实验周期设计合理的给药频率
参考文献:
[1] Chen Y, Liu X, Chen J, et al. Macrophage CCL7 promotes resistance to immunotherapy for colorectal cancer by regulating the infiltration of macrophages and CD8+ T cells. J Immunother Cancer. 2025;13(11):e013027. Published 2025 Nov 24. doi:10.1136/jitc-2025-013027
巨噬细胞清楚产品推荐
Absin产品线:
爆款产品:十大试剂盒(mIHC、IHC、凋亡、ELISA、ChIP、Co-IP、生化检测、残留检测、多因子检测);细胞培养(类器官试剂盒+基质胶,胎牛血清+培养添加剂+细胞因子)、分化试剂盒;分子(mRNA合成服务+提取试剂盒);化合物大包装;辅助试剂、耗材/仪器、定制服务(抗体/多肽/蛋白/标记/检测)...
特色产品:鸡胚提取物CEE、B27、N2、霍乱毒素B亚单位CTB、牛脑垂体提取物BPE、百日咳毒素PTX、重组人胰岛素Insulin、人源低密度脂蛋白LDL...
爱必信(上海)生物科技有限公司
联系邮箱:info@absin.cn
微信公众号:爱必信生物
.jpg)
相关新闻资讯