
7YR企业会员
发布人:爱必信(上海)生物科技有限公司
发布日期:2026/4/20 13:23:49
在肿瘤免疫治疗领域,抗原呈递缺陷一直是制约 T 细胞免疫疗法疗效的关键难题。肿瘤细胞因 MHC-I 分子相关抗原呈递不足,导致抗原性低、易发生抗原逃逸,让杀伤性 T 细胞难以精准识别并攻击肿瘤。近日,《Advanced Materials》发表的一项创新性研究,通过级联响应肽自组装介导 T 细胞抗原与喜树碱(CPT)的肿瘤靶向共递送,成功重塑肿瘤抗原性,为癌症免疫治疗提供了全新思路 —— 而 Absin 的优质产品,正是这一突破性研究的重要支撑。


研究团队针对肿瘤抗原呈递缺陷的核心痛点,设计了一套 “级联响应 + 靶向递送 + 协同治疗” 的三维策略:
级联响应肽载体设计:构建 PSA(Nap-GFFpYE-ss-Ag)和 CPSA(CPT-GFFpYE-ss-Ag)两种自组装肽载体,均含 ALP 响应的磷酸化四肽(-GFFpY-)和 GSH 可切割的二硫键(-ss-),实现 “胞外 ALP 去磷酸化触发组装→胞内 GSH 切割释放 cargo” 的精准调控。
双重活性成分递送:PSA 负载 OVA 来源的抗原表位 OVA₂₅₇₋₂₆₄,CPSA 在此基础上增加拓扑异构酶 I 抑制剂 CPT,既实现外源性抗原的靶向递送,又通过 CPT 增强 MHC-I 分子表达,双重提升肿瘤抗原呈递效率。
联合治疗增效:结合过继性 OT-I CD8⁺ T 细胞输注,同时利用 CPSA 诱导 PD-L1 表达的特性,联合抗 PD-L1 抗体(aPD-L1),形成 “抗原呈递增强 + T 细胞靶向激活 + 免疫检查点阻断” 的协同效应(图 1)。
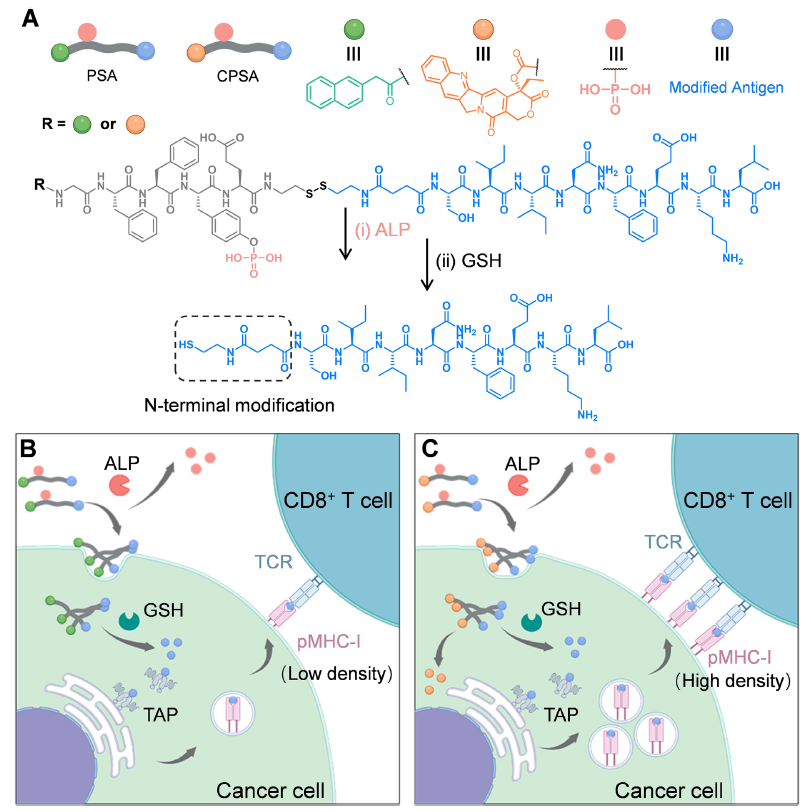
注:原文图 1,展示 PSA/CPSA 的化学结构、级联响应递送过程及抗原呈递机制,B、C 图由 BioRender 绘制
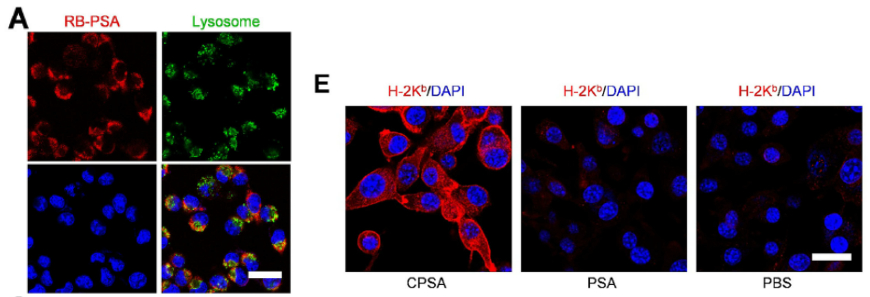
体外实验证实,PSA/CPSA 在 ALP 作用下发生去磷酸化,引发结构重构形成高密度纳米纤维(图 2A-D),60 分钟内去磷酸化率达 100%(图 2E);胞内 GSH 触发抗原持续释放,且 N 端延伸的 OVA₂₅₇₋₂₆₄与 H-2Kᵇ的结合稳定性显著优于原始抗原(图 2G-H)。
细胞摄取实验显示,PSA 通过动力蛋白依赖的内吞途径进入 MC38 细胞,成功逃逸溶酶体并在胞内形成自组装体(图 3A-C),抗原呈递效率随时间持续提升,12 小时后 H-2Kᵇ- 抗原复合物阳性率达 82.3%(图 3F)。
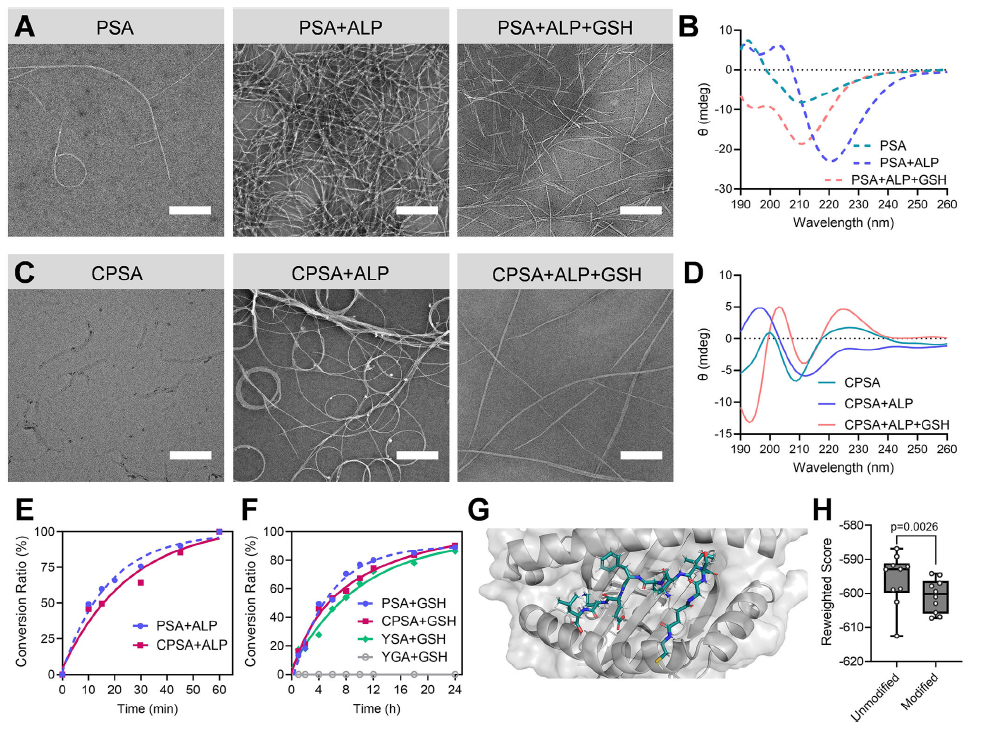
原文图 2,A-D 为 TEM 图像与 CD 光谱,E 为去磷酸化动力学,F 为抗原释放曲线,G-H 为抗原 - H-2Kᵇ结合模型
PSA/CPSA 处理的 MC38 细胞能高效招募 OT-I CD8⁺ T 细胞,细胞接触指数较未处理组提升 4.14 倍(图 3K-L),LDH 释放实验证实肿瘤细胞杀伤率显著提高(图 3M)。
CPSA 处理后,MC38 细胞的 H-2Kᵇ表达提升 1.81 倍,H-2Kᵇ- 抗原复合物表达提升 14.94 倍(图 5A-D),并促进 OT-I CD8⁺ T 细胞分泌 IFN-γ、IL-2、颗粒酶 B 等效应分子(图 5G-J)。
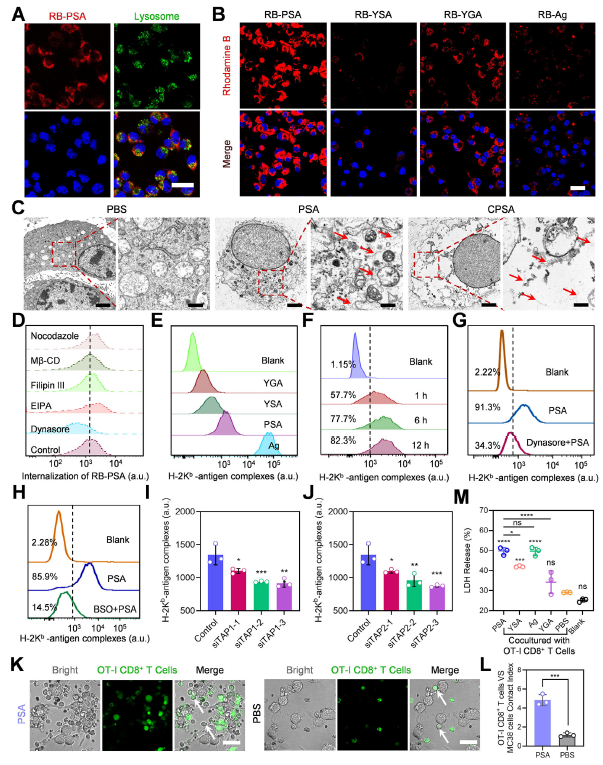
原文图 3,A 为 RB-PSA 细胞定位,B 为不同肽载体的细胞摄取,E 为抗原呈递水平,K-M 为 T 细胞靶向杀伤相关结果
荷 MC38 肿瘤小鼠模型中,PSA 静脉注射后能在肿瘤部位高效富集并持续留存 48 小时,肿瘤抑制率达 63.5%(图 4E-F);CPSA 联合 aPD-L1 治疗的肿瘤抑制率进一步提升至 74.5%(图 6C)。
免疫浸润分析显示,PSA/CPSA 治疗组肿瘤组织中 CD3⁺CD8⁺ T 细胞、颗粒酶 B⁺ CD8⁺ T 细胞等效应细胞浸润显著增加(图 4I-M、图 6F-I),证实疗法能有效激活抗肿瘤免疫应答。
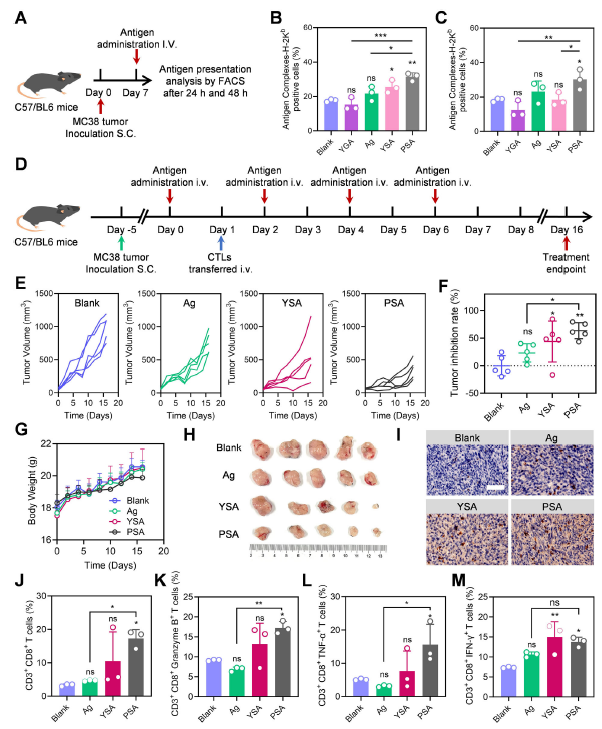
原文图 4,B-C 为体内抗原呈递水平,E-F 为肿瘤生长曲线与抑制率,I-M 为 T 细胞浸润分析
本研究的顺利开展,离不开 Absin 优质产品的稳定支持,其中兔抗 CD274 多克隆抗体(货号:abs115675)和抗荧光淬灭剂(货号:abs9235)发挥了重要作用:
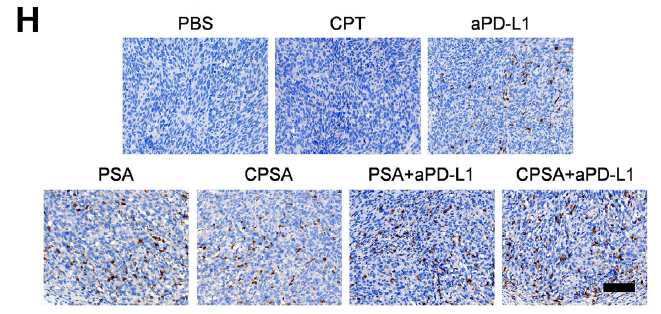
兔抗 CD274 多克隆抗体:特异性识别小鼠 PD-L1(CD274)蛋白,为验证 “CPSA 治疗上调 PD-L1 表达、增强免疫检查点阻断敏感性” 这一关键机制提供了可靠的检测工具,确保了 PD-L1 表达定量分析的准确性。
抗荧光淬灭剂:在细胞免疫荧光染色(如 H-2Kᵇ分子定位、T 细胞与肿瘤细胞相互作用观察)中,有效维持荧光信号稳定性,避免了因荧光淬灭导致的成像模糊或信号丢失,为 CLSM 图像的清晰采集提供了保障,助力研究者直观观察肽载体的细胞定位、抗原呈递及细胞间相互作用。
Absin 始终致力于为生命科学研究提供高品质试剂,从特异性抗体到实验辅助试剂,全方位满足科研需求,助力科研工作者突破技术瓶颈,加速创新成果转化。
本研究通过级联响应肽自组装技术,成功解决了肿瘤抗原呈递不足的核心问题,为 T 细胞免疫疗法与化疗、免疫检查点阻断的联合应用提供了全新范式。其创新之处在于:首次实现外源性抗原精准递送与 MHC-I 表达增强的双重调控,同时通过联合 aPD-L1 破解免疫抑制微环境,显著提升抗肿瘤疗效。
未来,该策略有望结合临床可用抗原(如新生抗原、公共抗原),拓展至 CAR-T、TCR-T 等疗法中,为人类癌症治疗提供更高效的精准免疫治疗方案。而 Absin 也将持续深耕科研试剂领域,以更优质的产品和服务,支撑更多前沿研究的开展,与科研工作者共同推动生命科学领域的进步!
本文内容基于《Advanced Materials》(DOI: 10.1002/adma.202516767)原文献;文中涉及的原文献图片、数据等知识产权归原期刊及研究团队所有。若存在侵权情形,敬请及时联系我方删除,我方将积极配合处理。
相关新闻资讯