
2YR企业会员
发布人:普健生物(武汉)科技有限公司
发布日期:2026/4/22 11:32:43
宠物医学正迎来精准靶向时代,从过敏瘙痒到肿瘤免疫逃逸,再到慢性肾病和骨关节炎,已锁定多个核心分子靶点。本文按疾病类别系统整理了常见宠物疾病和关键治疗靶点以及研究进展。
核心症状:剧烈瘙痒(pruritus)是犬特应性皮炎最突出临床表现,常表现为持续抓挠、舔咬、摩擦,导致局部皮肤红肿、丘疹、渗出,甚至苔藓化(lichenification)。长期抓挠易继发细菌或酵母菌感染(如马拉色菌),进一步加重炎症。皮肤屏障破坏是核心病理之一:表皮角质层脂质异常、丝聚蛋白(filaggrin)表达下调,导致经皮水分丢失增加,过敏原更容易侵入,形成恶性循环。
IL-4 / IL-4Rα (CD124):Th2炎症启动与IgE产生的核心开关。IL-4是一种经典Th2型细胞因子,主要由Th2细胞、肥大细胞和嗜碱性粒细胞分泌。在犬特应性皮炎中,过敏原刺激后,皮肤树突细胞(DC)捕获抗原并迁移至引流淋巴结,IL-4通过结合IL-4Rα(CD124,由IL-4Rα链和共同γ链或IL-13Rα1链组成)激活JAK1/JAK3-STAT6信号通路。
IL-31:JAK/STAT通路直接触发“痒觉开关”,IL-31是Th2细胞和肥大细胞分泌的“痒觉特异性”细胞因子,被称为“pruritogen(致痒因子)”。其受体复合物(IL-31RA + OSMRβ)高表达于皮肤感觉神经末梢、角质形成细胞、巨噬细胞和嗜酸性粒细胞。
SLAMF1 (CD150):2025年Mars Petcare Biobank新发现的遗传易感基因。SLAMF1(Signaling Lymphocytic Activation Molecule Family 1,又称CD150)是一种跨膜免疫调节受体,主要表达于T细胞、B细胞、NK细胞和树突细胞表面。其胞质尾部含有ITSM(immunoreceptor tyrosine-based switch motif)基序,可招募SAP(SLAM-associated protein)和Fyn激酶,形成SLAM-SAP-Fyn信号复合物,精细调控免疫细胞活化、增殖和耐受。
新型JAK抑制剂 Ilunocitinib(商品名Zenrelia™,Elanco):非选择性JAK抑制剂,对JAK1、JAK2和TYK2具有高亲和力。通过阻断多种Th2/致痒细胞因子(IL-2、IL-4、IL-6、IL-13、IL-31等)的下游JAK-STAT信号,实现“多靶点”抑制:直接阻断IL-31在感觉神经元上的信号 → 快速止痒(数小时内起效);抑制IL-4/IL-13/IL-6信号 → 减少Th2炎症、IgE产生和急性期反应;同时改善皮肤屏障相关炎症。药代动力学支持每日一次给药(半衰期约5小时,24小时内维持有效血药浓度)。
托珠单抗(Tocilizumab,人源化抗IL-6R单抗):IL-6是急性炎症和Th17/Th2放大过程中的关键细胞因子,通过结合膜型和可溶型IL-6R(mIL-6R/sIL-6R)激活经典和反式信号通路,促进炎症细胞因子风暴、急性期蛋白合成及B细胞活化。2025年体外研究证实,托珠单抗可特异性结合犬IL-6R,阻断IL-6介导的STAT3磷酸化,产生明显的抑制性生物反应(抑制下游炎症介质释放)。
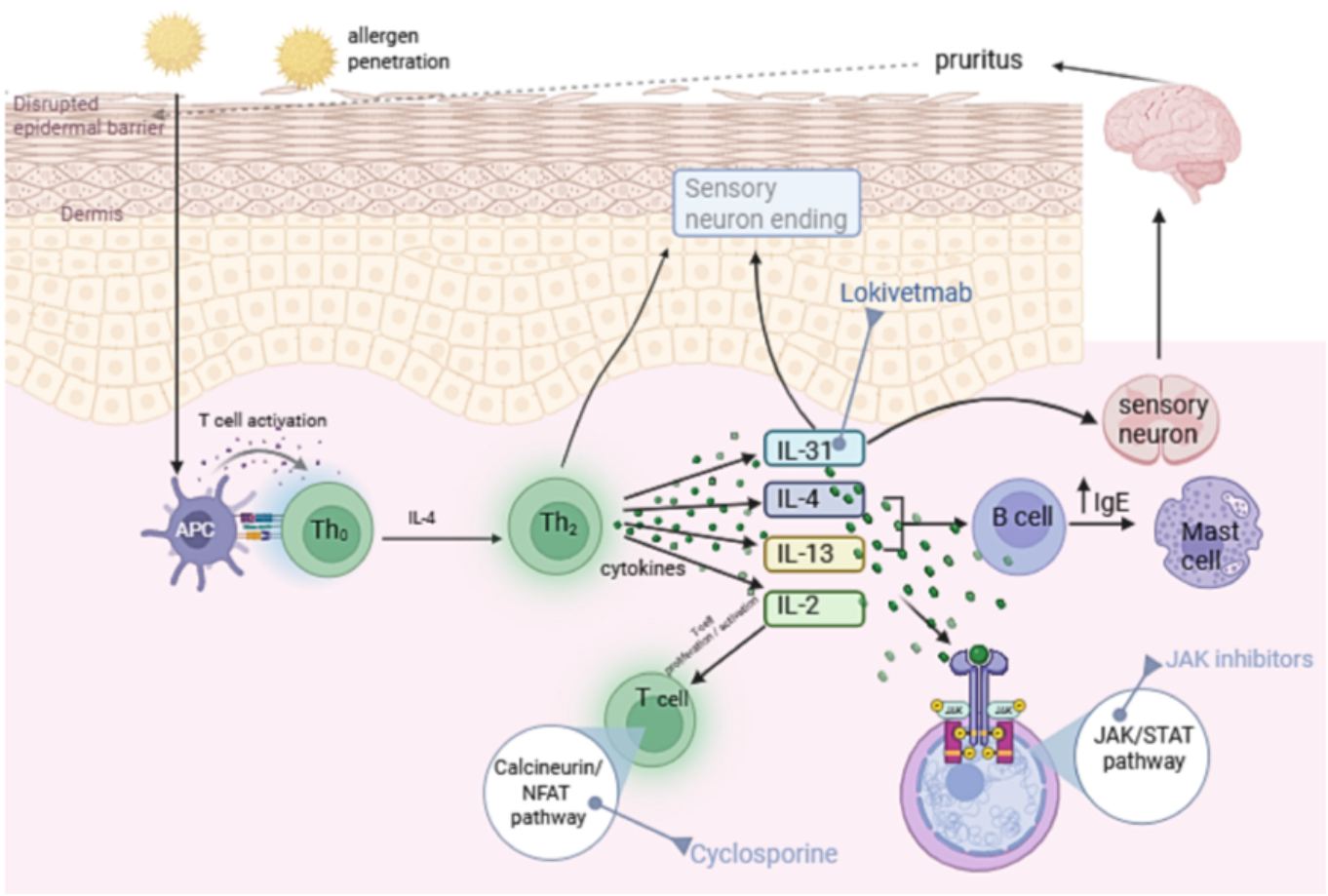
Figure 1. 犬变应性皮炎的免疫病理机制以及抗细胞因子疗法的药物靶点
核心症状:关节肿痛、活动受限(IMPA类似类风湿关节炎)、慢性腹泻/黏液便/体重减轻(IBD)、反复呕吐/腹痛/厌食(慢性胰腺炎),伴全身慢性炎症、发热及继发感染风险。
IL-6:炎症级联放大器与JAK/STAT激活中枢。由滑膜细胞、巨噬细胞及肠上皮细胞分泌,通过经典/反式信号激活JAK1/2-STAT3通路,促进Th17分化、MMPs表达、破骨细胞活化及肠道屏障破坏。在IMPA中导致滑膜炎症与关节破坏;在IBD中增强上皮通透性与腹泻;在慢性胰腺炎中放大腺泡细胞损伤与纤维化。犬猫IMPA/IBD患病动物滑膜液及血清IL-6水平显著升高。
TNF-α:黏膜/关节破坏的直接驱动因子。激活NF-κB/MAPK通路,诱导MMPs/ADAMTS表达降解软骨/黏膜基质,促进破骨细胞分化及肠上皮凋亡。在IMPA中驱动滑膜炎症;在IBD中加重蛋白丢失性肠病;在慢性胰腺炎中参与腺泡坏死与纤维化。
JAK/STAT通路:广谱炎症信号枢纽,阻断后可同时抑制Th17/Th1偏倚、MMPs表达及黏膜/关节炎症。
IL-1β:早期炎症与软骨/腺泡破坏主力,通过NF-κB诱导iNOS/NO及MMPs,在慢性胰腺炎中尤为关键。
IL-17:Th17驱动的骨/黏膜破坏因子,与TNF-α协同促进RANKL表达。
抗NGF单抗:Bedinvetmab(犬用,Librela®)和Frunevetmab(猫用,Solensia®),全犬源化/猫源化单抗特异性结合游离NGF,阻止其与TrkA/p75NTR结合,快速阻断外周和中枢痛觉敏化,同时减轻神经炎症和血管新生(不直接抑制经典炎症细胞因子)。
JAK抑制剂(Tofacitinib、Upadacitinib等):小分子口服药阻断JAK-STAT信号,广谱抑制IL-6、IL-2、IL-15、IFN-γ等多细胞因子转导,减少Th17分化、MMPs表达和破骨细胞活化;同时在肠道中修复黏膜屏障、减少腹泻。
抗IL-23/TNF-α双特异性抗体:针对犬猫IBD/OA,体外/动物模型显示同时阻断黏膜破坏和关节炎症,有望实现“one-drug-multiple-symptoms”治疗。
MSC(间充质干细胞)疗法:可下调IL-6/TNF-α,促进软骨再生,已在犬OA临床中显示良好耐受性。
Piclidenoson(A3腺苷受体激动剂):2026年Phase 2犬OA试验进行中,机制为抑制IL-17/IL-23轴,有望成为新型口服抗炎药。
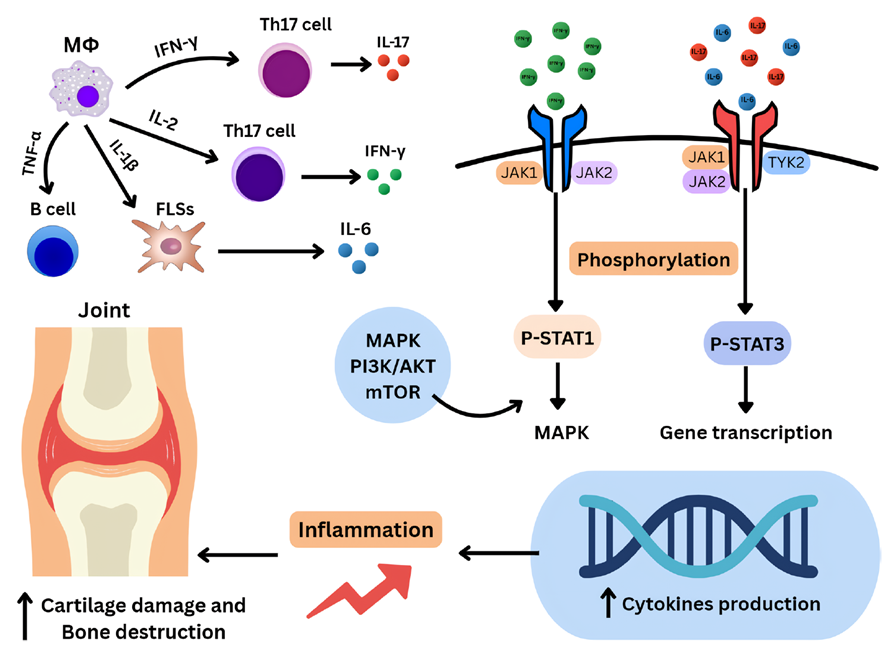
Figure 2. JAK STAT通路在类风湿关节炎中的作用
核心症状:口腔黑色素瘤、骨肉瘤、乳腺瘤、淋巴瘤、肥大细胞瘤、鳞状细胞癌等
PD-1/PD-L1:免疫检查点抑制的核心开关。肿瘤细胞上调PD-L1结合T细胞PD-1,抑制T细胞活化与细胞因子释放,实现免疫逃逸。在犬口腔黑色素瘤、肉瘤及猫乳腺癌中高表达。阻断后恢复T细胞杀伤活性。
c-KIT:酪氨酸激酶受体,犬肥大细胞瘤(MCT)驱动基因。常见外显子突变导致组成性激活,驱动细胞增殖、存活及血管新生。通过PI3K/AKT及MAPK通路促进肿瘤生长。
VEGF/VEGFR:血管新生关键因子。肿瘤分泌VEGF结合VEGFR,促进内皮细胞增殖与肿瘤血管形成,支持肿瘤生长与转移。
CTLA-4:T细胞共抑制分子。与CD28竞争B7配体,抑制早期T细胞活化;阻断后增强T细胞启动与记忆形成,与PD-1抑制剂协同。
PD-1抑制剂:犬源化抗PD-1单抗gilvetmab在MCT及黑色素瘤中肿瘤缩小或稳定率达60-73%;2025年多中心试验显示ca-4F12-E6在晚期口腔黑色素瘤中客观缓解率显著,联合抗CTLA-4(ca1C5)进一步增强疗效。猫用抗PD-1(1A1-2)证实可阻断PD-1/PD-L1并提升IFN-γ产生。
TKI酪氨酸激酶抑制剂:toceranib/masitinib针对c-KIT突变MCT,数据显示客观缓解率高;2026年新兴TKI(如sorafenib类似物)扩展至实体瘤。
其他:2026年猫乳腺癌全基因组研究发现FBXW7/PIK3CA突变,提示PI3K抑制剂潜在应用;UC Davis 2025年猫口腔鳞癌新药临床试验显示1/3患猫疾病控制,副作用低。
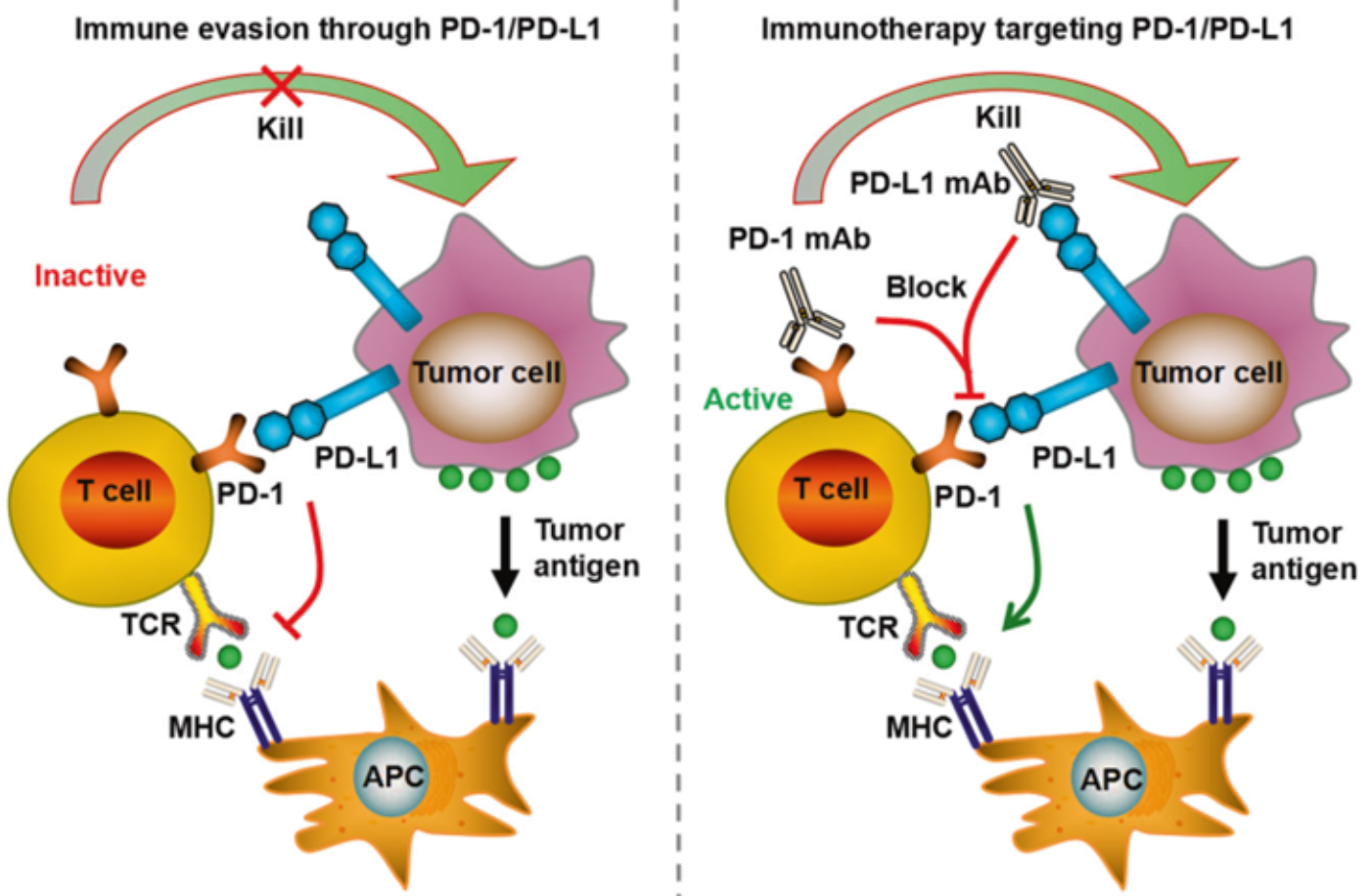
Figure 3. PD-1/PD-L1通路促进肿瘤免疫逃逸,使肿瘤能够抵抗免疫反应
核心症状:多饮多尿、食欲下降、贫血、高磷血症
RAAS(肾素-血管紧张素-醛固酮系统):核心血流动力学与纤维化驱动。肾小球滤过率下降激活肾素→Ang II→醛固酮,引起肾小球高压、蛋白尿及间质纤维化。Ang II还促进炎症与氧化应激。
FGF23 / Klotho:磷代谢失调与心脏-肾脏轴损伤。CKD早期FGF23升高,抑制磷重吸收及1,25-(OH)₂D合成,同时降低Klotho表达;FGF23直接激活RAAS并诱导左室肥厚。
SGLT2:近端小管葡萄糖/钠重吸收,抑制后减轻肾小球高压与炎症(人医已转化,兽医探索中)。
醛固酮:独立于Ang II的纤维化因子,加重肾小管损伤。
RAAS阻断仍是治疗基石:2025年IRIS指南推荐替米沙坦(ARB)作为蛋白尿和高血压一线药物,通过阻断Ang II受体,减轻肾小球高压、降低蛋白尿(UP/C下降)并抑制TGF-β纤维化。研究显示其在猫CKD中优于或不劣于贝那普利,与氨氯地平联合效果更佳。
替米沙坦联合SGLT2抑制剂类似物:2025-2026年探索显示,联合SGLT2抑制剂(如velagliflozin类似物)可通过激活管-球反馈,减轻肾小球高压和炎症,与RAAS阻断协同延缓GFR下降。目前主要用于猫糖尿病,早期CKD有肾保护潜力,需监测脱水。
FGF23 / Klotho靶向研究:2025年IDEXX FGF-23检测纳入IRIS猫CKD早期推荐。高FGF23通过与Klotho结合抑制磷重吸收和维生素D合成,导致磷潴留和RAAS激活。高水平预测进展与较差存活。目前靠磷结合剂+处方粮间接调控。
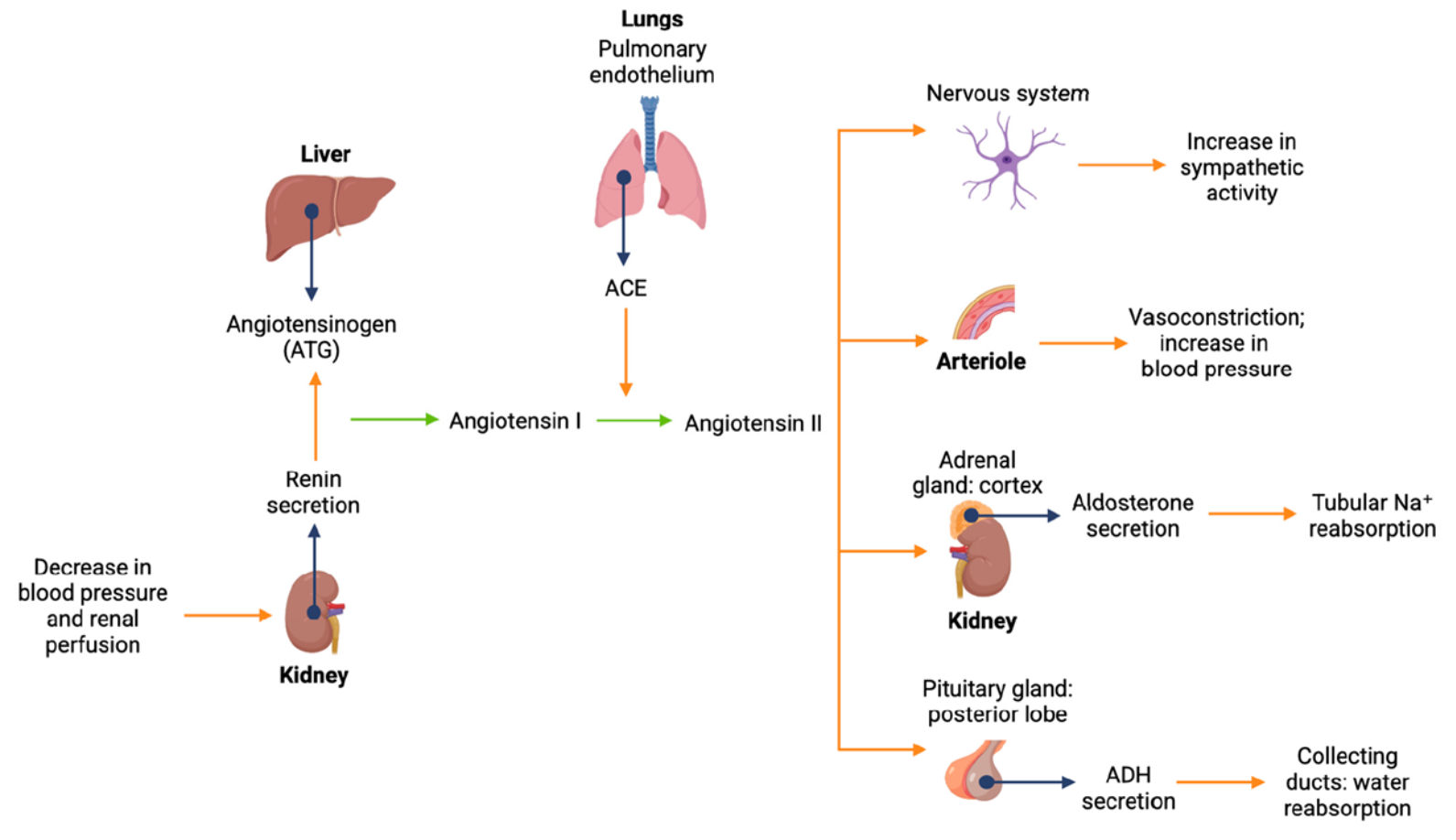
Figure 4. Schematic representation of the renin–angiotensin–aldosterone system (RAAS) and its main physiological effects.
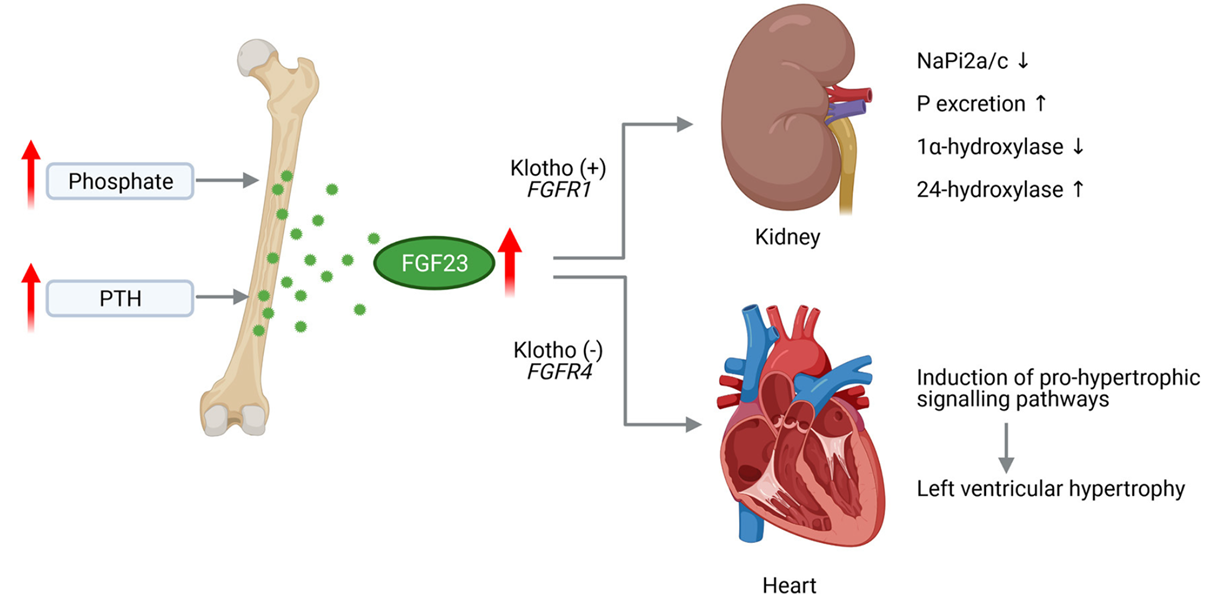
Figure 5. FGF23在CKD中对肾脏和心脏的病理影响
核心症状:心力衰竭(呼吸困难、咳嗽、运动不耐受、腹水)、动脉血栓形成(尤其是猫HCM导致的鞍状血栓,表现为后肢麻痹、疼痛、冷肢)、晕厥、心律失常,晚期可出现恶病质和猝死。
肌球蛋白(Myosin):猫HCM核心收缩异常靶点。MYBPC3基因突变(Maine Coon/Ragdoll常见)导致肌丝超收缩、左室流出道梗阻及心肌肥厚;阻断肌球蛋白ATPase可减少能量消耗与重构。
NT-proBNP:心脏壁应力标志物(非直接靶点但关键监测指标)。心室牵拉释放NT-proBNP,反映心肌负荷与心衰风险;在犬MMVD/DCM中用于鉴别心源性/呼吸性呼吸困难及预后评估。
cTnI(心肌肌钙蛋白I):心肌损伤标志物,反映心肌细胞损伤,在HCM及犬心肌病中升高提示预后不良。
肌球蛋白抑制剂:mavacamten/aficamten在猫模型中剂量依赖性降低左室流出道压力梯度与肥厚(Sharpe et al. 2025);2026年猫慢性给药试验进行中,有望转化。
雷帕霉素(rapamycin/sirolimus):NC State 2025年临床试验显示靶向制剂可逆转猫HCM症状(左室壁厚下降、心功能改善),2026年FDA扩大条件批准,真正“逆转”HCM的药物。
生物标志物指导:2025-2026年犬NT-proBNP/cTnI联合检测指南更新,>1500 pmol/L NT-proBNP可早期预测心衰风险;猫HCM筛查中NT-proBNP辅助基因检测(MYBPC3)。
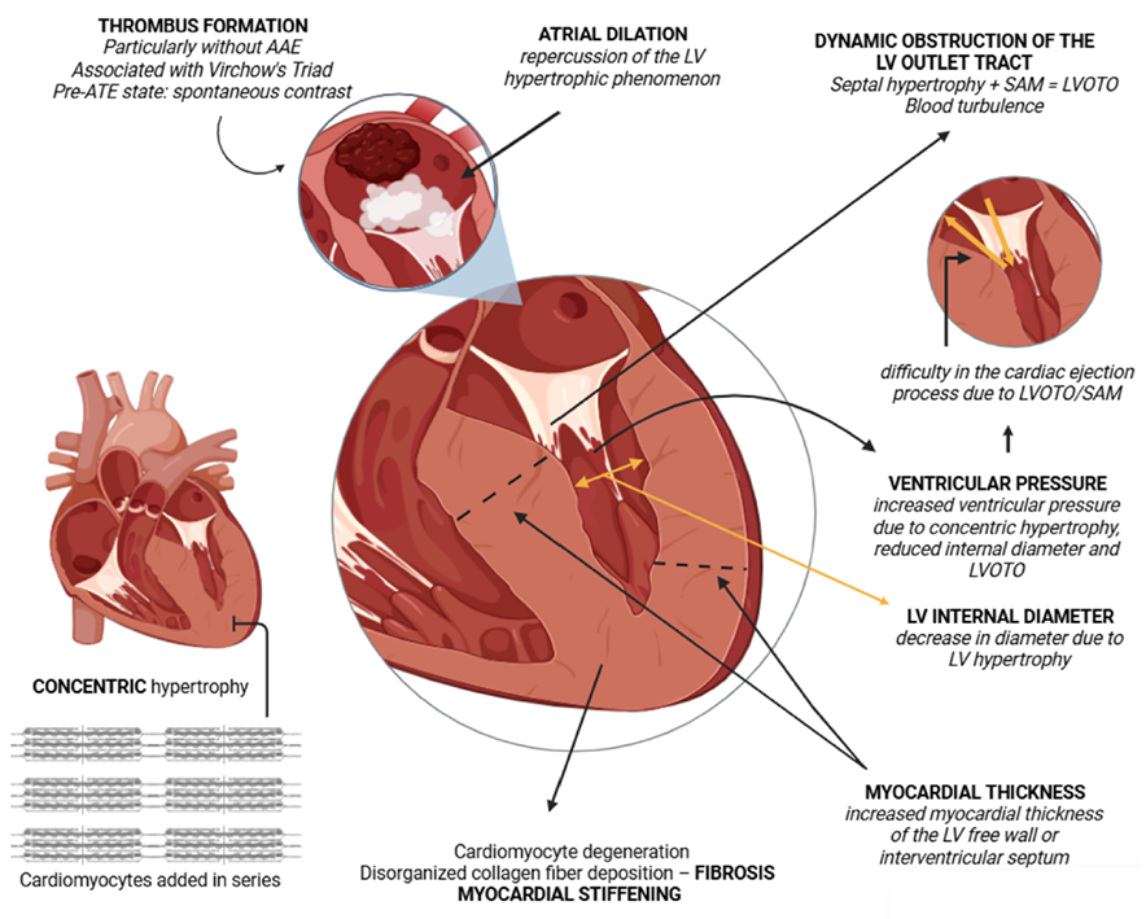
Figure 6. 猫肥厚型心肌病(HCM)表型的病理生理学示意图
核心症状:反复感染、生长迟缓、病毒性疾病(犬瘟热CDV、猫白血病FeLV)
CD150 / SLAMF1:病毒入侵免疫细胞的关键受体
CD132 / IL2RG:X连锁重症联合免疫缺陷(XSCID)致病基因
纳米抗体阻断CDV通过SLAM受体入侵;基因修复技术探索
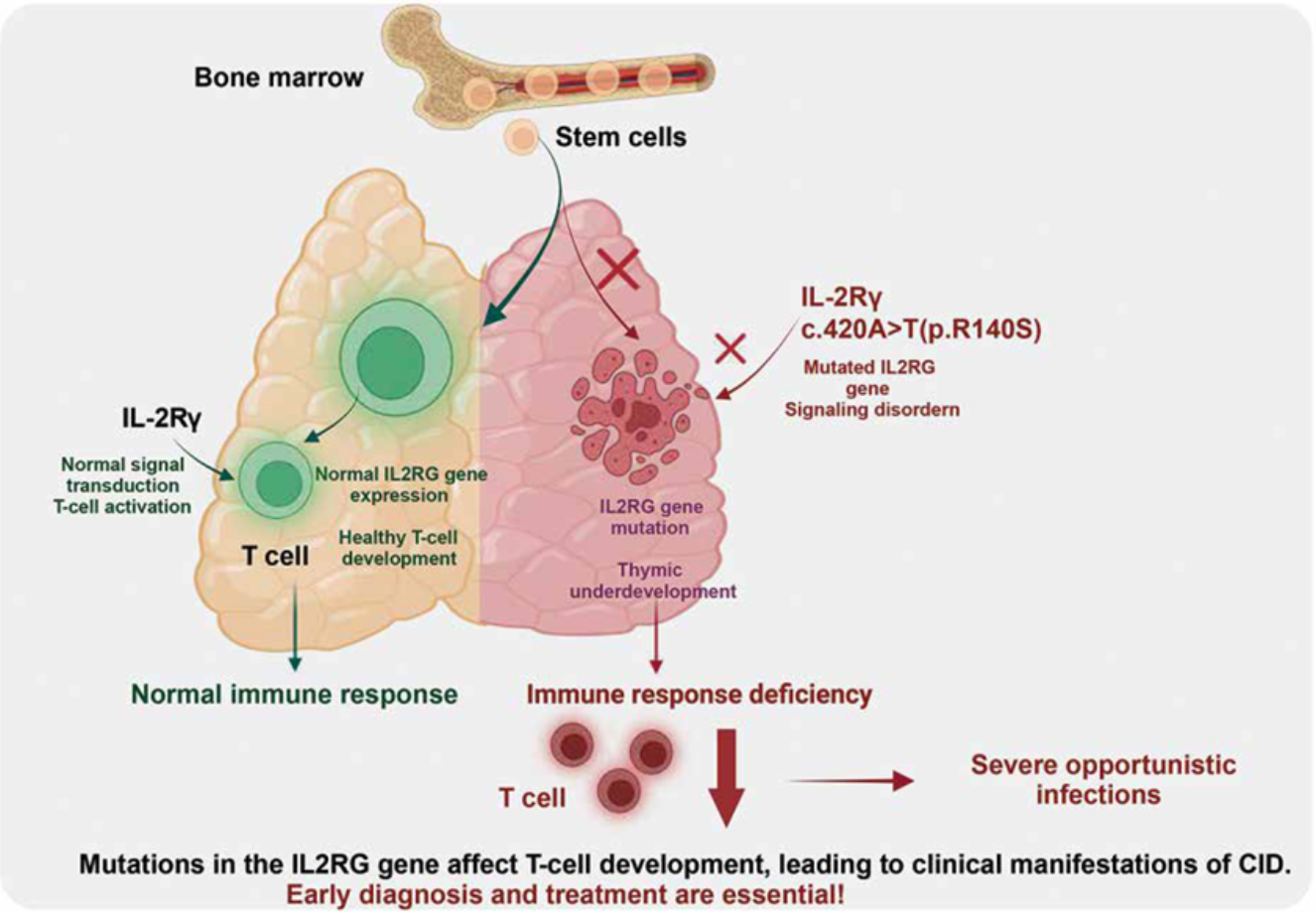
Figure 7. 新型IL2RG基因突变在原发性联合免疫缺陷中的机制
以下是abinScience提供的宠物相关治疗靶点的蛋白产品清单,更多产品可联系专员咨询!
1. Della Rocca G, Coaccioli S, Di Salvo A.
Beyond Osteoarthritis: Emerging Applications of Anti-NGF Monoclonal
Antibodies in Pain Management in Dogs and Cats. Animals (Basel). 2025
Nov 8;15(22):3243.
2. Luri-Rey C, Teijeira Á, Wculek SK, et al.
Cross-priming in cancer immunology and immunotherapy. Nat Rev Cancer.
2025 Apr;25(4):249-273.
3. Grund A, Sinha MD, Haffner D, et al.
Fibroblast Growth Factor 23 and Left Ventricular Hypertrophy in Chronic
Kidney Disease-A Pediatric Perspective. Front Pediatr. 2021 Aug
4;9:702719.
4. Merbl Y, Lopez Baltazar JM, Byron M, et al.
Tocilizumab binds to canine IL-6 receptor and elicits in-vitro
inhibitory biological response. Front. Vet. Sci. 12:1645414.
5. de
Sousa FG, Muzzi RAL, de Araújo RB, et al. Linking clinical and imaging
diagnostic assessments of the feline hypertrophic cardiomyopathy
phenotype. Front. Vet. Sci. 12:1720886.
6. Wichtowska A, Olejnik M.
Anti-Cytokine Drugs in the Treatment of Canine Atopic Dermatitis. Int J
Mol Sci. 2025 Nov 13;26(22):10990.
7. Di Palma Subran M, Wyss M,
Taskoparan B, et al. Nanobody-based canine PD-L1-targeting immune
checkpoint inhibitors for cancer therapy in dogs. Mol Ther Oncol. 2025
Sep 8;33(3):201036.
8. Cao F, Shi Y, Deng F, Yan Y. Novel IL2RG gene
mutation causing primary combined immunodeficiency disease: A case
report and literature review. Cent Eur J Immunol. 2024;49(3):300-307.
9.
Meng L, Wu H, Wu J, et al. Mechanisms of immune checkpoint inhibitors:
insights into the regulation of circular RNAS involved in cancer
hallmarks. Cell Death Dis. 2024 Jan 4;15(1):3.
10. Kiełbowski K,
Plewa P, Bratborska AW, et al. JAK Inhibitors in Rheumatoid Arthritis:
Immunomodulatory Properties and Clinical Efficacy. Int J Mol Sci. 2024
Jul 30;25(15):8327.
11. Forster S, Trout CM, Despa S, et al. Efficacy
and field safety of ilunocitinib for the control of atopic dermatitis
in client-owned dogs: A multicentre, double-masked, randomised,
placebo-controlled clinical trial. Vet Dermatol. 2025 Oct;36(5):647-659.
相关新闻资讯