在生物制药领域,中国仓鼠卵巢(CHO)细胞是重组蛋白、单克隆抗体等生物药生产的核心表达系统,全球 70% 以上的重组蛋白药物均由 CHO 细胞生产,堪称生物制药的 “超级细胞工厂”。但在药物生产过程中,CHO 细胞会同步分泌多种内源性蛋白,这些非目标蛋白杂质被称为 CHO 宿主细胞蛋白(CHO HCP),其残留量直接关系到生物药的安全性、有效性与合规性,是生物药质量控制体系中不可或缺的检测指标。
一、CHO HCP 的定义、产生与核心危害
(一)定义与产生
CHO HCP 是 CHO 细胞在培养、增殖及目标蛋白生产过程中,分泌或释放到细胞培养基、细胞上清及生物工艺样本中的内源性蛋白质杂质。作为生物制药中最主要的工艺相关杂质,CHO HCP 的产生具有必然性:CHO 细胞在正常生理代谢、生长增殖过程中会合成自身所需的各类蛋白,在细胞裂解、发酵过程中,这些蛋白会被释放到培养体系中;即便经过下游纯化工艺,仍可能有微量 HCP 残留,成为影响药物质量的 “隐形风险”。
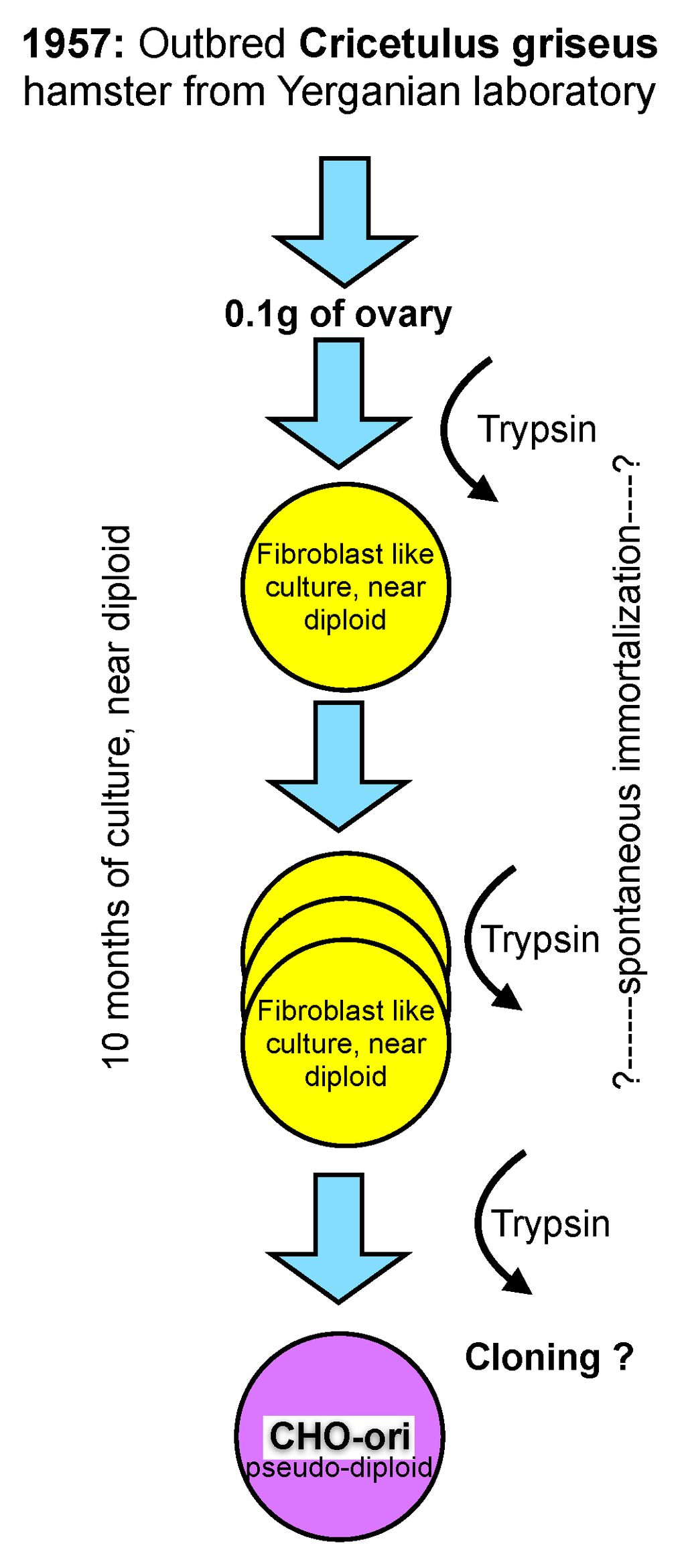
早期 原始 CHO 细胞系的构建过程。https://doi.org/10.3390/pr1030296
(二)核心危害
CHO HCP 作为外源蛋白,其残留会给生物药带来多重安全与质量风险,也是各国药监部门重点管控的对象:
1.免疫原性风险:CHO HCP 作为外来物质,可能引发人体免疫反应,产生抗 HCP 抗体,轻则导致过敏反应,重则通过 “佐剂效应” 增强抗药抗体(ADA)的产生,影响药物的药代动力学与治疗效果,甚至引发严重免疫损伤;
2.生物学干扰风险:部分 CHO HCP 具有酶活性、细胞因子活性等生物学功能,即使微量残留,也可能干扰人体正常生理过程,如诱导免疫细胞异常分化、引发炎症反应等;
3,药物质量影响:部分酶类 HCP 可能降解目标药物成分或辅料,促进药物聚集,影响药物稳定性,导致药物在储存过程中失效或产生有害物质。
二、CHO HCP 检测的必要性与法规要求
CHO HCP 的残留控制是生物药合规生产与质量保障的核心环节,各国药监部门均制定了严格的限值要求,明确规定生物药生产过程中需对 CHO HCP 进行精准检测与严格控制:
国际法规:ICH Q6B 指南、美国药典(USP)<1132> 章节均要求,生物药中 CHO HCP 残留量通常需低于 100 ppm(即 1mg 总蛋白中 HCP 含量小于 100ng);
中国法规:《中国药典》(2025 版)明确规定,CHO 细胞来源的生物药中,HCP 残留量需不高于蛋白质总量的 0.05%(500 ppm),远低于大肠杆菌等其他表达系统的限值要求,凸显其管控重要性。
此外,在生物药研发、工艺优化、批次质量验证等环节,CHO HCP 的定量检测也是评估纯化工艺效率、保障产品批次一致性的关键手段,直接决定药物研发进度与生产合规性。
三、CHO HCP 检测技术特点与优势
传统 CHO HCP 检测方法(如 ELISA)存在操作繁琐、洗涤步骤多、检测周期长、样本消耗量较大等弊端,难以适配高通量生物药研发与生产质控的需求。而 TR-FRET(时间分辨荧光共振能量转移)技术的应用,彻底解决了这一痛点,成为 CHO HCP 精准检测的优选技术。
TR-FRET 技术结合了时间分辨荧光与荧光共振能量转移的双重优势,通过供体(铕螯合物)与受体荧光染料的特异性结合,可有效消除背景荧光干扰,具有高灵敏度、高特异性、均相免洗、操作快速等特点,仅需微量样本即可实现精准定量,完美适配生物药生产中不同阶段(细胞培养、纯化、成品)的样本检测需求,大幅提升检测效率与数据可靠性。
四、CHO HCP 精准检测解决方案:THUNDER™ CHO Host Cell Protein TR-FRET Assay Kit
针对生物药研发与生产中 CHO HCP 的定量检测需求,THUNDER™ CHO Host Cell Protein TR-FRET Assay Kit 依托夹心 TR-FRET 均相免疫技术,为科研与生产用户提供高效、精准、合规的检测工具,适配细胞培养基、细胞上清及生物工艺样本的检测场景。产品链接:THUNDER- CHO Host Cell Protein TR-FRET Assay Kit_Bioauxilium_优宁维(univ)商城
该试剂盒核心优势突出,全面满足生物药质控的严苛要求:采用均相免洗检测体系,无需繁琐洗涤步骤,操作简便快速,大幅缩短检测周期;仅需 15 μL 微量样本即可实现高灵敏度检测,同时具备优异的特异性、稳健性与重复性,可有效避免非特异性结合带来的干扰;选用高品质抗体对,经严格研发、验证与质量控制测试,确保批次间检测结果一致,保障数据可靠;提供 5 种灵活规格,可满足不同通量实验需求,同时支持批量订购,兼顾科研效率与成本效益。
